- Studiu CDC privind monitorizarea siguranței unei doze suplimentare de vaccin COVID-19
- Ceea ce se știe deja despre thEști împușcat?
- Dintre 306 de participanți la studiile clinice Pfizer-BioNTech, reacțiile adverse după doza 3 au fost similare cu cele după doza 2.
Ce se adaugă în acest raport la împușcătura numărul 3 lansată astăzi de CDC?
În perioada 12 august - 19 septembrie 2021, printre 12,591 3 de persoane înregistrate în siguranță v care au finalizat un sondaj de sănătate după toate cele 19 doze de vaccin mARN COVID-79.4, 74.1% și 77.6% au raportat reacții locale sau sistemice, respectiv, după a treia doză; 76.5% și XNUMX% au raportat reacții locale sau sistemice după a doua doză, respectiv.
Care sunt implicațiile pentru practica de sănătate publică?
Rapoartele voluntare către v-safe nu au găsit modele neașteptate de reacții adverse după o doză suplimentară de vaccin COVID-19. CDC va continua să monitorizeze siguranța vaccinului, inclusiv pentru dozele suplimentare de COVID-19.
La 12 august 2021, Food and Drug Administration (FDA) a modificat autorizațiile de utilizare de urgență (EUA) pentru vaccinurile Pfizer-BioNTech și Moderna COVID-19 pentru a autoriza administrarea unei doze suplimentare după finalizarea unei serii de vaccinare primară persoanelor eligibile cu afecțiuni imunodeprimante moderate până la severe (1,2). La 22 septembrie 2021, FDA a autorizat o doză suplimentară de vaccin Pfizer-BioNTech ≥ 6 luni după finalizarea seriei primare la persoanele cu vârsta ≥ 65 de ani, cu risc crescut de COVID-19 sever sau a căror expunere profesională sau instituțională le pune la risc crescut pentru COVID-19 (1). Rezultatele unui studiu clinic de fază 3 efectuat de Pfizer-BioNTech care a inclus 306 persoane cu vârste cuprinse între 18 și 55 de ani au arătat că reacțiile adverse după primirea unei a treia doze administrate la 5-8 luni după finalizarea unei serii de vaccinare primară cu 2 doze de ARNm au fost similare cu cele raportate după primirea dozei 2; aceste reacții adverse au inclus ușoară până la moderată la locul injectării și reacții sistemice (3). CDC a dezvoltat v-safe, un sistem de supraveghere a siguranței voluntar, bazat pe smartphone, pentru a furniza informații despre reacțiile adverse după vaccinarea COVID-19.
Coincident cu autorizarea unei doze suplimentare pentru persoanele cu afecțiuni imunodeprimante, platforma v-safe a fost actualizată pentru a permite înregistranților să introducă informații despre dozele suplimentare de vaccin COVID-19 primite. În perioada 12 august - 19 septembrie 2021, un total de 22,191 de persoane înregistrate în condiții de siguranță v au raportat primirea unei doze suplimentare de vaccin COVID-19. Cei mai mulți (97.6%) au raportat o serie primară de vaccinare cu ARNm cu 2 doze urmată de o a treia doză din același vaccin. Dintre cei care au completat un studiu de sănătate pentru toate cele 3 doze (12,591; 58.1%), 79.4% și 74.1% au raportat reacții locale sau sistemice, respectiv, după doza 3, comparativ cu 77.6% și 76.5% care au raportat local sau sistemic. reacții, respectiv, după doza 2. Aceste constatări inițiale nu indică modele neașteptate de reacții adverse după o doză suplimentară de vaccin COVID-19; majoritatea acestor reacții adverse au fost ușoare sau moderate. CDC va continua să monitorizeze siguranța vaccinului, inclusiv siguranța dozelor suplimentare de vaccin COVID-19, și să furnizeze date care să ghideze recomandările vaccinului și să protejeze sănătatea publică.
V-safe este un sistem de supraveghere a siguranței SUA voluntar, bazat pe smartphone; persoanele vaccinate eligibile pentru a primi produs vaccinal autorizat sau autorizat se pot înregistra în v-safe. Platforma v-safe permite înregistranților existenți să raporteze că primesc o doză suplimentară de vaccin COVID-19 și noilor solicitanți să introducă informații despre toate dozele de vaccin COVID-19 primite. Sondajele de sănătate V-safe sunt trimise în zilele 0-7 după fiecare doză de vaccin și includ întrebări despre locul de injectare local și reacțiile sistemice și impactul asupra sănătății. * Sondajele sunt trimise pentru cea mai recentă doză introdusă.† Membrii personalului din sistemul de raportare a evenimentelor adverse pentru vaccin (VAERS) contactează persoanele înregistrate care indică faptul că a fost solicitată asistență medicală după vaccinare și încurajează sau facilitează completarea unui raport VAERS, dacă este indicat.§
Dintre persoanele înregistrate în siguranță v care au raportat primirea unei doze suplimentare de vaccin COVID-19 în perioada 12 august - 19 septembrie 2021, datele demografice, reacțiile locale și sistemice și efectele asupra sănătății raportate în zilele 0-7 au fost descrise în funcție de modelul de vaccinare (adică , producător de vaccin primit pentru fiecare doză). Persoanele care au raportat că primesc o serie primară de la diferiți producători sau de la un producător necunoscut sau indisponibil în Statele Unite sau 2 doze de vaccin după primirea unui vaccin cu doză unică Janssen (Johnson & Johnson) (150) au fost excluse din analiză de reacții adverse după primirea dozei suplimentare.
Timpul scurs de la finalizarea seriei de vaccinare primară până la primirea unei doze suplimentare a fost descris după modelul de vaccinare. Profilurile de evenimente adverse după dozele 2 și 3 au fost comparate pentru persoanele înregistrate care au primit vaccin ARNm de la același producător pentru toate cele 3 doze.¶ Software-ul SAS (versiunea 9.4; SAS Institute) a fost utilizat pentru efectuarea tuturor analizelor. Aceste activități de supraveghere au fost examinate de CDC și desfășurate în conformitate cu legislația federală aplicabilă și politica CDC. **
În perioada 12 august - 19 septembrie 2021, un total de 22,191 de persoane înregistrate în siguranță v-safe au raportat primirea unei doze suplimentare de vaccin COVID-19 după finalizarea seriei primare (Tabelul 1). Dintre aceștia, 14,048 (63.3%) au fost femei și aproximativ 30% au avut fiecare vârsta cuprinsă între 18-49, 50-64 și 65-74 ani.
Majoritatea persoanelor înregistrate (21,662; 97.6%) au raportat că au primit a treia doză de la același producător ca seria lor primară de vaccin ARNm, inclusiv 98.6% dintre beneficiarii Moderna și 98.2% dintre beneficiarii Pfizer-BioNTech. Puțini solicitanți (341; 1.5%) au raportat o serie de vaccinuri primare ARNm urmată de o doză suplimentară de vaccin ARNm de la un alt producător, o doză de vaccin Janssen după primirea unei serii primare de vaccinare ARNm (10; 0.05%) sau o suplimentare doza de vaccin COVID-19 de la orice producător după vaccinul Janssen (178; 0.8%).
Dintre cei 22,191 de persoane înregistrate în condiții de siguranță v, intervalul mediu de la finalizarea seriei primare de vaccinare COVID-19 până la primirea unei doze suplimentare a fost de 182 zile (intervalul interquartil [IQR] = 160-202 zile) (Tabelul 2). Dintre cei care au primit 2 doze de vaccin Janssen, intervalul mediu între doze a fost mai scurt (84 zile; IQR = 16-136 zile).
Reacțiile locale (16,615; 74.9%) și sistemice (15,503; 69.9%) au fost raportate frecvent în timpul săptămânii după o doză suplimentară de vaccin COVID-19, cel mai frecvent în ziua următoare vaccinării. Reacțiile raportate frecvent au fost durerea la locul injectării (15,761; 71.0%), oboseala (12,429; 56.0%) și cefaleea (9,636; 43.4%).
Dintre 22,191 de doze suplimentare, un total de 7,067 (31.8%) au raportat efecte asupra sănătății și aproximativ 28.3% (6,287) au raportat că nu au putut efectua activități zilnice normale, cel mai frecvent în ziua următoare vaccinării. Asistența medicală a fost solicitată de 401 (1.8%) persoane înregistrate, iar treisprezece (0.1%) au fost spitalizate. Motivele pentru care s-a primit îngrijire medicală sau spitalizare nu au fost identificate în sondajul v-safe; cu toate acestea, solicitanții care indică faptul că a fost solicitată asistență medicală după vaccinare sunt contactați de personalul VAERS și încurajați să completeze un raport VAERS.
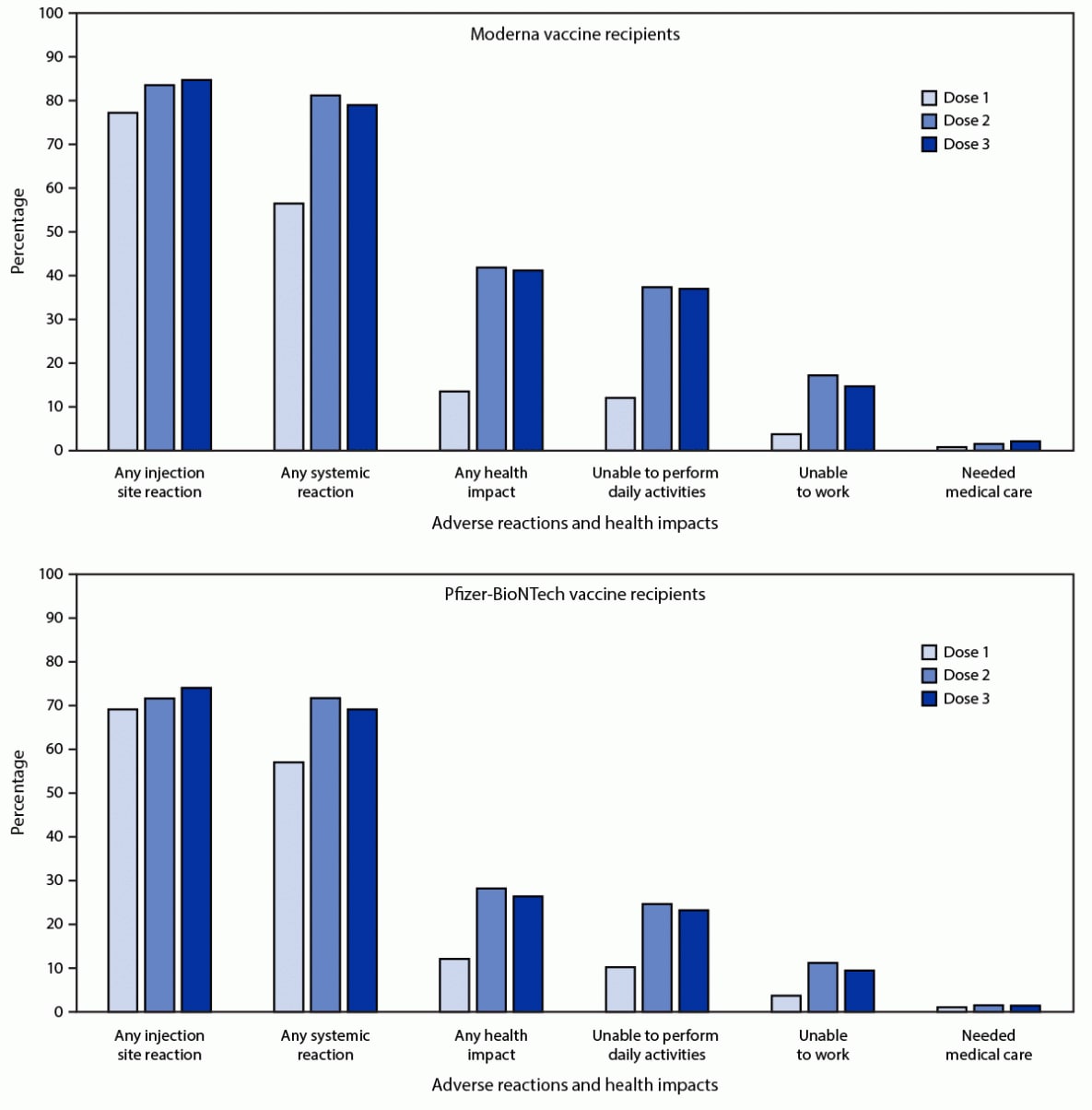
Dintre 21,658 de persoane înregistrate în condiții de siguranță v care au primit același vaccin ARNm pentru toate cele 3 doze, 12,591 (58.1%) au finalizat cel puțin un studiu de sănătate în zilele 0-7 după toate cele 3 doze; 79.4% și 74.1% au raportat reacții locale sau sistemice, respectiv, după doza 3, comparativ cu 77.6% și 76.5% care au raportat reacții locale sau sistemice, respectiv, după doza 2. Printre solicitanții care au primit 3 doze de Moderna (6,283), reacțiile au fost raportate mai frecvent după doza 3 decât doza 2 (5,323; 84.7% și 5,249; 83.5%; valoarea p = 0.03) (Figura). Reacțiile sistemice au fost raportate mai rar după doza 3 decât doza 2 (4,963; 79.0% și 5,105; 81.3%; valoarea p <0.001).
Dintre persoanele înregistrate care au primit 3 doze de Pfizer-BioNTech (6,308), reacțiile locale au fost raportate mai frecvent după doza 3 decât doza 2 (4,674; 74.1% și 4,523; 71.7%; valoarea p <0.001). Reacțiile sistemice au fost raportate mai rar după doza 3 decât doza 2 (4,363; 69.2% și 4,524; 71.7%; valoarea p <0.001). Dintre cei care au raportat durere după doza 3 a unui vaccin ARNm, cele mai multe reacții au fost ușoare (4,909; 51.4%) sau moderate (4,000; 41.9%); durerea severă (definită ca durere care face dificile sau imposibile activitățile zilnice) a fost raportată de 637 (6.7%).
Discuție
Începând cu 19 septembrie 2021, aproximativ 2.21 milioane de persoane din Statele Unite primiseră doze suplimentare de vaccinuri COVID-19†† după finalizarea unei serii primare. În perioada 12 august - 19 septembrie 2021, nu s-au observat modele neașteptate de reacții adverse în rândul celor 22,191 de persoane înregistrate în siguranță v care au primit o doză suplimentară de vaccin COVID-19. Cele mai multe reacții locale și sistemice raportate au fost ușoare până la moderate, tranzitorii și cel mai frecvent raportate în ziua următoare vaccinării. Majoritatea solicitanților care au primit o doză suplimentară au raportat o serie primară de vaccinare cu ARNm urmată de o a treia doză de la același producător.
Studiul clinic Pfizer-BioNTech, care a inclus 306 persoane cu vârste cuprinse între 18 și 55 de ani, a arătat că reacțiile după doza 3 au fost comparabile cu cele raportate după doza 2 (3). Cu toate acestea, această analiză a datelor v-safe a constatat că reacțiile locale au fost puțin mai frecvente și reacțiile sistemice mai puțin frecvente după doza 3 de Pfizer-BioNTech.
Modelele reacțiilor adverse observate după doza 3 de vaccin Moderna sau Pfizer-BioNTech au fost în concordanță cu reacțiile descrise anterior după primirea dozei 2
Numărul persoanelor înregistrate care au indicat că au primit 2 doze de vaccin Janssen sau au primit doza suplimentară de la un producător diferit de cel din seria lor primară a fost mic, limitând orice concluzii.
Datele privind siguranța sau eficacitatea vaccinării cu produse vaccinale COVID-19 de la diferiți producători sunt limitate; Comitetul consultativ pentru practicile de imunizare (ACIP) recomandă persoanelor cu condiții de imunocompromisie moderată până la severă să primească o a treia doză de vaccin mRNA COVID-19 de la același producător ca și seria lor primară.
Recomandările CDC pentru o doză suplimentară nu includ în prezent persoanele care au primit vaccinul Janssen.
În perioada acoperită de acest studiu, recomandările ACIP pentru o doză suplimentară de vaccin COVID-19 au fost limitate la persoanele cu afecțiuni imunocompromise moderate până la severe care au primit
2 doze de vaccin mARN.
Un studiu efectuat la pacienții cu hemodializă imunodeprimată a raportat că reacțiile locale și sistemice după doza 3 de vaccin Pfizer-BioNTech au fost similare cu cele după doza 2.¶¶ Raportările recente privind infecțiile la persoanele vaccinate și creșterea prevalenței infecției cu varianta B.1.617.2 (Delta) a SARS-CoV-2, virusul care provoacă COVID-19, în rândul persoanelor vaccinate ar fi putut determina unele persoane să caute o doză suplimentară în afara recomandărilor. Intervalul median de la finalizarea seriei primare până la primirea unei doze suplimentare a fost de aproximativ 6 luni; prin urmare, persoanele prioritizate în timpul lansării vaccinurilor COVID-19, inclusiv lucrătorii din domeniul sănătății și adulții în vârstă, ar fi putut primi o doză suplimentară.
Constatările din acest raport sunt supuse a cel puțin patru limitări. În primul rând, înscrierea în v-safe este voluntară și probabil că nu este reprezentativă pentru populația vaccinată din SUA; majoritatea participanților s-au identificat ca fiind albi și non-hispanici. În al doilea rând, în timpul acestei perioade de studiu, recomandările suplimentare privind dozele au fost limitate la persoanele cu afecțiuni imunodeprimante care au finalizat o serie primară de vaccinare cu ARNm COVID-19; cu toate acestea, v-safe nu include informații despre starea imunitară.
Beneficiarii de doze suplimentare includ probabil persoane cu sau fără afecțiuni imunodeprimante. În al treilea rând, nu se poate stabili o relație de cauzalitate între un vaccin și un eveniment advers clinic grav raportat după vaccinare, utilizând date v-safe. În cele din urmă, datele insuficiente au fost disponibile pentru a determina modelele reacțiilor adverse după primirea unei doze suplimentare de la un producător diferit de seria primară sau pentru vaccinul Janssen.
O doză suplimentară de vaccin mRNA COVID-19 este recomandată persoanelor cu afecțiuni imunocompromise moderate până la severe (5).
CDC a recomandat o doză suplimentară de vaccin Pfizer-BioNTech ≥ 6 luni după finalizarea seriei de vaccin primar la persoanele cu vârsta ≥ 65 de ani, rezidenții aflați în medii de îngrijire pe termen lung și persoanele cu vârsta cuprinsă între 50 și 64 de ani cu afecțiuni medicale subiacente; persoanele cu vârste cuprinse între 18 și 49 de ani cu afecțiuni medicale subiacente și persoanele cu vârste cuprinse între 18 și 64 de ani cu risc crescut de expunere și transmitere a COVID-19 din cauza cadrului profesional sau instituțional pot primi o doză suplimentară în funcție de beneficiile și riscurile lor individuale
Analizele inițiale ale datelor de siguranță de la> 22,000 de persoane înregistrate în siguranță v arată că reacțiile locale sunt ușor crescute și reacțiile sistemice sunt ușor scăzute după doza 3 a unui ARNm decât după doza 2.
Nu au fost identificate modele neașteptate de reacții adverse; cele raportate au fost ușoare până la moderate și trecătoare. CDC va continua să monitorizeze siguranța dozelor suplimentare de vaccin COVID-19. Datele suplimentare despre reacțiile adverse asociate cu diferite combinații de vaccinuri și cu timpul de la finalizarea seriei primare vor fi importante pentru a ghida recomandările de sănătate publică.
| Caracteristică | Moderna,%† (n = 10,601) | Pfizer-BioNTech,%† (n = 11,412) | Janssen,%†, § (n = 178) | Total (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Doza 3 Moderna (n = 10,453; 98.6%) | Doza 3 Pfizer-BioNTech (n = 144; 1.4%) | Doza 3 Janssen (n = 4; 0.04%) | Doza 3 Pfizer-BioNTech (n = 11,209; 98.2%) | Doza 3 Moderna (n = 197; 1.7%) | Doza 3 Janssen (n = 6; 0.1%) | Doza 2 Janssen (n = 48; 27.0%) | Doza 2 Moderna (n = 64; 36.0%) | Doza 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| sex | ||||||||||
| Femeie | 63.8 | 63.9 | 50.0 | 63.0 | 63.5 | 33.3 | 39.6 | 57.8 | 59.1 | 63.3 |
| Masculin | 35.1 | 34.0 | 50.0 | 36.1 | 36.0 | 66.7 | 60.4 | 42.2 | 40.9 | 35.7 |
| Necunoscut | 1.0 | 2.1 | 0 | 0.9 | 0.5 | 0 | 0 | 0 | 0 | 1.0 |
| Grupa de vârstă, an | ||||||||||
| 0-17 | 0.0 | 0.7 | 0.0 | 0.6 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.3 |
| 18-49 | 25.7 | 36.1 | 25.0 | 31.5 | 42.6 | 50.0 | 54.2 | 60.9 | 57.6 | 29.1 |
| 50-64 | 28.4 | 27.1 | 50.0 | 31.1 | 29.9 | 0.0 | 33.3 | 34.3 | 30.3 | 29.8 |
| 65-74 | 33.9 | 27.1 | 0.0 | 27.8 | 21.3 | 50.0 | 10.4 | 4.7 | 9.1 | 30.5 |
| 75-84 | 10.9 | 9.0 | 25.0 | 8.3 | 5.6 | 0.0 | 2.1 | 0.0 | 3.0 | 9.5 |
| ≥ 85 | 1.1 | 0.0 | 0.0 | 0.7 | 0.5 | 0.0 | 0.0 | 0.0 | 0.0 | 0.9 |
| Etnie | ||||||||||
| Hispanic / Latino | 8.0 | 15.3 | 0 | 8.2 | 5.6 | 0 | 25.0 | 6.3 | 10.6 | 8.2 |
| Non-hispanici / latino | 87.7 | 81.9 | 100 | 87.6 | 90.9 | 100 | 54.2 | 89.1 | 89.4 | 87.6 |
| Necunoscut | 4.3 | 2.8 | 0 | 4.2 | 3.6 | 0 | 20.8 | 4.7 | 0 | 4.2 |
| Rasă | ||||||||||
| AI / AN | 0.5 | 0.7 | 0 | 0.5 | 0.5 | 0 | 2.1 | 0 | 0 | 0.5 |
| Asiatic | 4.9 | 5.6 | 0 | 6.1 | 7.1 | 0 | 2.1 | 14.1 | 13.6 | 5.6 |
| Negru | 5.6 | 3.5 | 0 | 6.2 | 1.5 | 16.7 | 6.3 | 6.3 | 9.1 | 5.9 |
| NHPI | 0.2 | 0 | 0 | 0.3 | 0.5 | 0 | 4.2 | 0 | 0 | 0.3 |
| Alb | 82.6 | 82.6 | 100 | 80.4 | 85.8 | 66.7 | 56.3 | 71.9 | 69.7 | 81.4 |
| multirascial | 1.9 | 2.1 | 0 | 1.8 | 1.5 | 16.7 | 4.2 | 4.7 | 3.0 | 1.9 |
| Altele | 2.1 | 4.2 | 0 | 2.1 | 0.5 | 0 | 6.3 | 1.6 | 3.0 | 2.1 |
| Necunoscut | 2.3 | 1.4 | 0 | 2.5 | 2.5 | 0 | 18.8 | 1.6 | 1.5 | 2.4 |
Abrevieri: AI / AN = indian american / nativ din Alaska; NHPI = Nativ hawaian sau alt insular din Pacific.
* Procentul de solicitanți care au finalizat cel puțin un sondaj de sănătate v-safe în zilele 0-7 după vaccinare.
† Seria de vaccinare primară.
§ Include persoanele care au primit o doză unică primară Janssen și o doză suplimentară de vaccin de la producătorii enumerați.
| Reacţie | Moderna,%† (n = 10,477) | Pfizer-BioNTech,%† (n = 11,284) | Janssen,%†, § (n = 174) | Total (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Doza 3 Moderna (n = 10,453; 98.6%) | Doza 3 Pfizer-BioNTech (n = 144; 1.4%) | Doza 3 Janssen (n = 4; 0.04%) | Doza 3 Pfizer-BioNTech (n = 11,209; 98.2%) | Doza 3 Moderna (n = 197; 1.7%) | Doza 3 Janssen (n = 6; 0.1%) | Doza 2 Janssen (n = 48; 27.0%) | Doza 2 Moderna (n = 64; 36.0%) | Doza 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| Zile de la seria primară, mediană (IQR) | 182 (164 - 198) | 183 (161 - 204) | 173 (141 - 182) | 183 (157 - 209) | 186 (161 - 217) | 123 (113 - 182) | 84 (16 - 136) | 156 (140 - 164) | 150 (136 - 167) | 182 (160 - 202) |
| Orice reacție la locul injectării | 80.9 | 64.6 | 75.0 | 69.4 | 81.7 | 83.3 | 25.0 | 70.3 | 80.3 | 74.9 |
| Mâncărime | 20.0 | 11.8 | 0 | 8.4 | 10.2 | 16.7 | 10.4 | 6.3 | 7.6 | 13.9 |
| Durere | 75.9 | 60.4 | 75.0 | 66.6 | 80.2 | 83.3 | 20.8 | 68.8 | 74.2 | 71.0 |
| Roşeaţă | 25.2 | 8.3 | 0 | 9.8 | 20.8 | 16.7 | 6.3 | 7.8 | 12.1 | 17.1 |
| Umflătură | 33.6 | 17.4 | 0 | 16.8 | 30.5 | 16.7 | 6.3 | 12.5 | 18.2 | 24.8 |
| Orice reacție sistemică | 75.2 | 59.7 | 50.0 | 65.1 | 76.1 | 100 | 31.3 | 68.8 | 63.6 | 69.9 |
| Durere abdominală | 8.4 | 3.5 | 0 | 6.4 | 8.1 | 16.7 | 4.2 | 3.1 | 6.1 | 7.3 |
| mialgie | 49.8 | 29.2 | 0 | 36.3 | 49.2 | 50.0 | 20.8 | 45.3 | 33.3 | 42.7 |
| Frisoane | 31.3 | 8.3 | 50.0 | 17.5 | 33.5 | 50.0 | 8.3 | 23.4 | 10.6 | 24.1 |
| Diaree | 9.9 | 7.6 | 0 | 9.0 | 9.6 | 16.7 | 8.3 | 6.3 | 9.1 | 9.4 |
| Oboseală | 61.8 | 44.4 | 0 | 51.0 | 60.9 | 83.3 | 14.6 | 48.4 | 50.0 | 56.0 |
| Febră | 36.4 | 20.1 | 50.0 | 22.2 | 37.1 | 50.0 | 6.3 | 37.5 | 12.1 | 29.0 |
| Durere de cap | 49.0 | 31.1 | 0 | 38.4 | 49.7 | 83.3 | 18.8 | 35.9 | 40.9 | 43.4 |
| Dureri articulare | 33.0 | 18.8 | 0 | 23.0 | 31.0 | 33.3 | 16.7 | 20.3 | 19.7 | 27.7 |
| Greaţă | 18.8 | 10.4 | 25.0 | 13.6 | 21.3 | 33.3 | 8.3 | 9.4 | 18.2 | 16.1 |
| Eritem | 2.3 | 0.7 | 0 | 1.9 | 2.5 | 0 | 4.2 | 1.6 | 1.5 | 2.1 |
| Vărsături | 2.2 | 2.1 | 25.0 | 1.4 | 2.0 | 0 | 2.1 | 0 | 0 | 1.7 |
| Orice impact asupra sănătății | 39.2 | 19.4 | 0 | 25.2 | 39.1 | 33.3 | 16.7 | 28.1 | 24.2 | 31.8 |
| Incapacitatea de a efectua activități zilnice normale | 35.2 | 18.1 | 0 | 22.1 | 33.0 | 33.3 | 10.4 | 25.0 | 15.2 | 28.3 |
| Incapacitatea de a lucra sau de a merge la școală | 13.7 | 4.9 | 0 | 9.0 | 21.3 | 16.7 | 10.4 | 6.3 | 13.6 | 11.3 |
| Aveți nevoie de îngrijire medicală | 2.1 | 1.4 | 0 | 1.5 | 3.0 | 0 | 6.3 | 0 | 0 | 1.8 |
| telehealth | 0.9 | 0.7 | 0 | 0.7 | 1.0 | 0 | 2.1 | 0 | 0 | 0.8 |
| clinică | 0.7 | 0.7 | 0 | 0.6 | 0.5 | 0 | 4.2 | 0 | 0 | 0.6 |
| Vizită de urgență | 0.2 | 0 | 0 | 0.2 | 0 | 0 | 4.2 | 0 | 0 | 0.2 |
| Spitalizare | 0.05 | 0 | 0 | 0.1 | 0 | 0 | 0 | 0 | 0 | 0.1 |
FIGURA. Reacții adverse și impacturi asupra sănătății raportate de persoanele care au primit 3 doze * de vaccin Moderna (N = 6,283) sau Pfizer-BioNTech (N = 6,308) COVID-19 și au completat cel puțin un sondaj de sănătate v-safe în zilele 0– 7 după fiecare doză, după numărul dozei - Statele Unite, 12 august - 19 septembrie 2021
CE ESTE DE LUAT DIN ACEST ARTICOL:
- Results from a phase 3 clinical trial conducted by Pfizer-BioNTech that included 306 persons aged 18–55 years showed that adverse reactions after receipt of a third dose administered 5–8 months after completion of a 2-dose primary mRNA vaccination series were similar to those reported after receipt of dose 2.
- Persons who reported receiving a primary series from different manufacturers or a manufacturer that was unknown or unavailable in the United States, or 2 doses of vaccine after receipt of a Janssen (Johnson &.
- On August 12, 2021, the Food and Drug Administration (FDA) amended Emergency Use Authorizations (EUAs) for the Pfizer-BioNTech and Moderna COVID-19 vaccines to authorize administration of an additional dose after completion of a primary vaccination series to eligible persons with moderate to severe immunocompromising conditions (1,2).























